NaCl型結晶の近接イオンの数 [CVX-化学発展演習 日記]
こんにちは~ (*^_^*)/
東大などでしばしば難問の出題される結晶ですが、今回はイオン結晶の配位数について考えてみましょう。
頻出の岩塩型(塩化ナトリウム型・NaCl型)について考えてみましょう。
設問
「塩化ナトリウム型結晶において、① 1個のナトリウムイオンは何個の塩化物イオンと接しているか? また、② 1個のナトリウムイオンに2番目に近いイオン(第2近接イオン),③ 第3近接イオン,④ 第4近接イオン の数はそれぞれ何個か?」
設問にあわせて、ナトリウムイオンを中心とするモノを考えてみます。
1個のイオンに接するイオン(最近接イオン)の数を配位数と言います。上記の単位格子の場合、単位格子の面の中心にいる塩化物イオン(緑色の球)が中心のナトリウムイオンと接している最近接イオンになります。中心のナトリウムイオンとそれに接する塩化物イオンだけを取り出してみると次のようになります。
塩化物イオンの中心を線で結んでみると、正八面体になるので、正八面体構造といいます。よって、①の配位数(最近接イオンの数)は6個です。このように、最近接イオンは、必ず異符号のイオンとなり、NaCl型では6個が配位することになります。
さて、次は②の第2近接イオンと③の第3近接イオンについて考えてみましょう。
単位格子から、中心のナトリウムイオンに接する塩化物イオン(最近接イオン)を取り除いた図が上の図です。こうしてみると、第2近接のナトリウムイオン(灰色の球)と第3近接の塩化物イオン(緑色の球)の位置関係がよく分かります。
第2近接イオンだけを考えてみると、面心立方構造の配置になっています。中心のナトリウムイオンを除いた図を見ると、第2近接のナトリウムイオンは12個であることが分かりますね。よって、②の第2近接イオンの数は12個となります。 これは、金属結晶の面心立方の配位数と同じです。第2近接イオンは、必ず同符号のイオンになります。
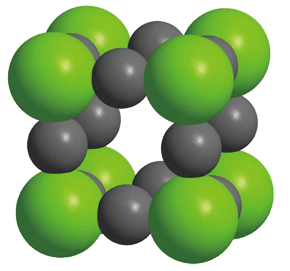
更に、単位格子から、中心のナトリウムイオンに対する最近接イオン,第2近接イオンを取り除いた図が、次の図です。
これを見ると、第3近接イオンは次の図のように、単位格子の各頂点の塩化物イオンです。立方体の頂点ですから、全部で8個ですね。よって、③の第3近接イオンの数は8個となります。第3近接イオンは異符号のイオンです。
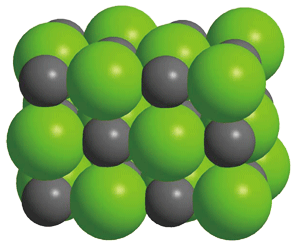
さて、単位格子中で中心のナトリウムイオンから最も遠くにある塩化物イオンが第3近接イオンですから、第4近接イオンは単位格子中には含まれないことになります。下図のように、4番目に遠いのは隣の単位格子の中心にある同符号のイオンであるナトリウムイオンだと分かります。
単位格子は正六面体(立方体)ですから、隣の単位格子は全部で6つあります。よって、④の第4近接イオンの数は6個になります。
結晶問題は、なるべく図を見て、その特性を掴むようにしましょう。難関医系受験では、スピードが勝負ですから、こういった出題パターンが決まっているモノは、覚えてしまった方が良いです。
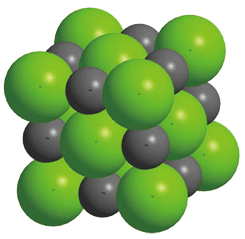
 正八面体構造
正八面体構造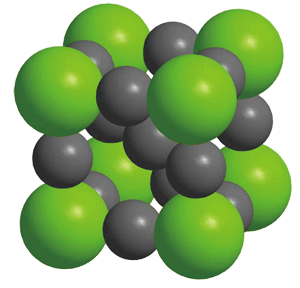





コメント 0