陰イオンの検出 [C3J-東大化学 日記]
こんにちは~ (*^_^*)/
前回に引き続き、無機テスト演習の補完です。 11月3日には有機化学のテスト演習(構造決定スペシャル)を行いますのでふるって参加して欲しいですね。
今回は、陰イオンの検出法と分離についてまとめました。講義で投影した映像の一部を交えて、簡単に解説しましょう。
大学入試で出題される陰イオンの主な区別の仕方は以下の通りです。 有色なイオンは水溶液の色から判断できますが、無色透明なイオンは、呈色反応や沈殿などで判別します。
陽イオンの系統分離と同様に、陰イオンにも系統的な分離があります。基本は、バリウムイオンや銀イオンとの沈殿の有無、および生じたバリウム塩の溶解性、銀塩の沈殿の有無による分離ですね。見慣れないので難しく感じるかもしれませんがも、実際には陽イオンの分離実験に比べて、分離に使用する試薬が少なく、(少なくとも入試での出題では)実験操作も簡単ですよ。
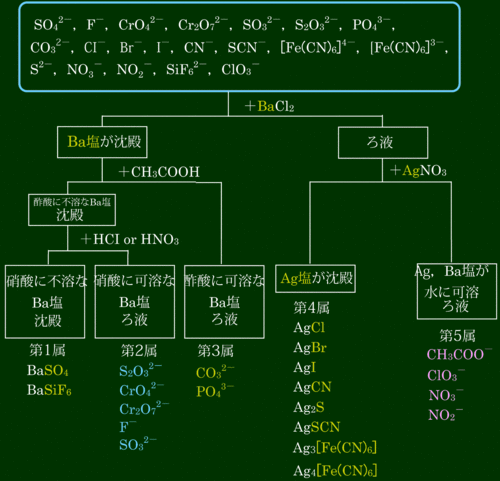
一通りの陰イオンを分離させていますが、大学入試で出題されるものだけに絞って分類すると、以下のようになります。
硫酸イオンは、沈殿を生じる陽イオンが少なく、アルカリ土類金属と鉛イオンだけです。水銀イオンや銀イオンとも沈殿を生じません。
クロム酸イオンや二クロム酸イオンは色だけで判別できるでしょう。クロム酸イオンは、2011年慶應義塾大学医学部でも出題されたように、 沈殿滴定で指示薬として使用されることが多いですね。ちなみに、クロム酸塩の沈殿で赤褐色なモノは、銀イオンだけじゃないことを知っていますよね?

炭酸イオンやリン酸イオンは、アルカリ金属を除く大半の金属イオンと沈殿を生じる陰イオンです。 共に弱酸の塩なので、強酸によって弱酸の遊離が起こり溶解します。ちなみにフェノールは炭酸ナトリウム水溶液には発泡せずに溶解することを知っていますよね?
鉄のシアノ錯イオンは有色なので判断しやすいですね。硫化物の基本色は黒なので、沈殿が黒ければ硫化物と考えて良いでしょう(例外は硫化亜鉛など)。ハロゲン化銀の色も頻出なので、しっかりと覚えておきましょう。特にヨウ化銀は、溶解度積が極めて小さいため、過剰アンモニアにもほとんど溶けません。
硝酸塩で水に溶けないモノはない。 だから、陽イオンの系統分離では硝酸塩を使います。そこで、硝酸イオンの検出には、硫酸鉄(Ⅱ)水溶液と濃硫酸を使った褐輪反応による呈色を行います。これについては、次の機会にまとめることにしましょう。
苦手な分野を集中して特訓するには、個別指導とテスト演習の組み合わせが効果的です。短期間で克服したい分野がある方は検討しては如何でしょう。








はじめまして。なおぽんと申します。
細かいところまでとても詳しく解説されているので度々お世話になっております!
いきなりの質問で申し訳ないのですが、この記事のクロム酸塩の沈殿所に書いてある、「銀イオン以外の赤褐色沈殿」というものを色々と調べてみたのですが、見つかりませんでした。
もしよろしければ、答えを教えていただけませんでしょうか?
お返事お待ちしております。
by なおぽん (2013-10-07 21:46)